Antibiograma_Esp Micro_UddfdfdfdfNFV.pptx
- 1. Antibiograma Edgar Gonzales Escalante SEGUNDA ESPECIALIDAD EN MICROBIOLOGÍA Actividad en Sede I
- 3. • Son métodos in vitro que determinan la sensibilidad antimicrobiana, las cuales deben reunir condiciones de laboratorio específicas y estandarizadas • Están indicados para cultivos bacterianos clínicamente relevantes (por ejemplo: fluidos normalmente estériles o sitios clínicamente infectados) cuando la susceptibilidad no puede ser predicha. • Enterobacterales, Pseudomonas, Acinetobacter, Estafilococos, Enterococos, Neumococos y Neisserias. Prueba de sensibilidad antimicrobiana
- 4. El antibiograma tiene como objetivo evaluar en el laboratorio la respuesta de un microorganismo a uno o a varios antimicrobianos, y traducir, en una primera aproximación, su resultado como factor predictivo de la eficacia clínica Antibiograma Es una de las funciones más importantes de los laboratorios de microbiología clínica.
- 5. Prueba de susceptibilidad antimicrobiana Clasificación según el resultado obtenido: • MÉTODOS CUANTITATIVOS Son aquellos procedimientos que permiten determinar la concentración inhibitoria mínima (CIM) y la concentración bactericida mínima (CBM). • MÉTODO CUALITATIVOS Son aquellos procedimientos que permiten microorganismo como sensible o resistente. clasificar directamente a un
- 7. Método Disco Difusión: Prueba de Kirby- Bauer Disco filtro impregnado con antibiótico. Prueba de susceptibilidad para mas de un antibiótico midiendo el tamaño de la “zona de inhibición”. 1949: Bondi y col. disco de papel 1966: Kirby, Bauer, Sherris, y Tuck Demostraron que los resultados cualitativos del metodo disco difusión Método Disco Difusión
- 8. Sir Alexander Fleming 1881-1955 Saint Mary Hospital in London Penicillium Staphylococcus aureus Fleming, A. On the antibacterial action of cultures of a penicillium, with special reference 1928 Historia
- 9. B A C Vincent & Vincent – 1944 – Uso de discos (papel filtro) impregnados con Redish ( 1928 ) - Uso de pocillos en el agar para antisépticos. Método Disco Difusión. Historia Mohs – 1945 - uso de cilindros de vidrio y metálicos
- 10. Historia Bauer, Kirby, Sherris y Turch, “Antibiotic susceptibility testing by standardized single disk method.” Am J Clin Pathol Ericsson, H. Hogman K. y Wickman K. “A paper disk method for determination of bacterial sensitivity to chemotherapeutic and antibiotic agents “ Scand. J. Clin. Lab. Invest.., 1954;
- 11. Método de disco difusión • En 1975, la NCCLS (actualmente la CLSI) adopto los pasos básicos del procedimiento descrito en el estudio de Kirby, Bauer y col. de 1966.
- 12. Procedimiento del metodo disco difusion • Prepara el inoculo del cultivo de la placa primaria, tocando con una asa o hisopo 3 a 5 colonias, de apariencia similar del microorganismo a probar. Selección de colonias y preparación del inoculo
- 13. Procedimiento del metodo disco difusion • Transferir este crecimiento a un tubo con solución salina. Luego comparar el tubo con la escala de Mc Farland 0.5 y ajustar la turbidez adicionando mas bacterias o mas solución salina estéril. PATRON DE TURBIDEZ: • Agregar 0,5 ml de una solución de BaCl2 0,048 M (BaCl2.2H2O al 1,175% P/V) a 99,5 mL de una solución de H2SO4 0,18 M (0,36 N) (1% V/V). • Verificar la densidad usando un espectrofotómetro, cuya absorbancia a 625 nm es 0,08 a 0,10. • Distribuir de 4 ml a 6 ml en tubos con tapa rosca o tapón de jebe, similares a los que se usarán para preparar el inóculo. • Guardar a temperatura ambiente, protegido de la luz (duración 6 meses).
- 14. Escala 0,5 Macfarlán (1,5 x 108 UFC/ml) Tubo Problema Tubo Patrón Absorbancia 0,08 – 0,10 a 625 nm Procedimiento del metodo disco difusion
- 15. Procedimiento del metodo disco difusion • Inocular la placa introduciendo el hisopo en el inoculo (remover el exceso en la pared del tubo). Estriar el hisopo sobre la superficie del medio 3 veces rotando la placa un ángulo de 60°. Retirar el exceso de muestra Estriamos en 3 Direcciones “Suspensión uniforme”
- 16. Procedimiento del metodo disco difusion • Los discos de antibióticos pueden ser colocados sobre la placa inoculada usando: pinzas estériles, una plantilla o un dispensador de discos de antibióticos.
- 17. Procedimiento del metodo disco difusion • Las placas deberían ser colocadas en la incubadora (en ambiente o en campana con CO2) dentro de los 30 minutos de su preparación. Bacterias fastidiosas requieren el uso de medios enriquecidos y de condiciones propias para su posterior interpretación.
- 18. Procedimiento del metodo disco difusion Medidas de la zona de inhibición: • Usando una regla: medir bajo la superficie de la placa conteniendo el medio transparente. • Usando un Vernier (pie de rey): medir sobre la superficie de la placa conteniendo el medio opaco.
- 19. Luz transmitida Luz reflejada Procedimiento del metodo disco difusion
- 22. • Medio de cultivo • Composición • Profundidad • pH • Cationes • El inoculo • Temperatura de incubación • Tamaño y carga del disco Factores que influyen en el tamaño de la zona de inhibición
- 23. Composición del agar • Agar Mueller Hinton • Buena reproducibilidad y bajo nivel de inhibidores. • Satisfactorio crecimiento para la mayoría de patógenos. • Almacenar en refrigeración (4-8 ° C). • Duración: de 7 hasta 14 días sellados con parafilm o en bolsas. • Realizar control de esterilidad y calidad.
- 24. Profundidad del Medio de cultivo 4 mm 2 mm 6 mm Profundidad aceptable: 4 ± 0,5 mm
- 25. Calculo del volumen de la placa Si ϴ = 9 cm » 25.4 ml Si ϴ = 10 cm » 31.4 ml Si ϴ = 15 cm » 70.6 ml OJO: “Diferentes marcas de placas, diferentes diámetros” Vol = π . r2 . h Vol agar = 3.14 x ( r )2 x 0.4 cm r = radio de la placa Petri Tolerancia: ± 0.5 cm (3.5 – 4.5)
- 26. pH del Medio de cultivo pH aceptable: 7.2 – 7.4 Medición en el agar
- 27. Densidad del Inoculo bacteriano Escala de Mc Farland 0.5
- 28. Densidad del Inoculo bacteriano Mc farland 1.0 Mc farland 0.5 Mc farland 0.3
- 29. Tamaño y peso de los discos Medida del disco = 6.18 mm Peso de un disco = 9 mg Área del disco = π.r2 A = 3.1416 x (3.09) 2 A = 29,9963 mm2 A = 0,2999 cm2 9 mg 1 cm2 30.01 mg Peso de los discos Estándares para los discos Code of Federal Regulations 1 cm2 papel filtro del disco = 30 mg ± 4
- 30. Control de calidad en el antibiograma: disco difusión • El uso correcto y exacto del antibiograma es dependiente de un buen control de calidad. • Control de calidad: reactivos, medio, procedimiento y competencia del personal. • Resultados del paciente no deberían ser entregados si los resultados de las cepas de control de calidad están fuera de las especificaciones.
- 31. Cepas patrón para el control de calidad: • Staphylococcus aures ATCC 25923 • Escherichia coli ATCC 25922 • Pseudomonas aeruginosa ATCC 27853 • Escherichia coli ATCC 35218 • Enterococcus faecalis ATCC 29212 El control de calidad se debe hacer: • Cada semana o cada 5 lotes de pruebas • Cada nuevo lote del agar Mueller Hinton • Cada nuevo lote de discos. Control de calidad en el antibiograma: disco difusión
- 34. Control de calidad en el antibiograma: disco difusión
- 35. Cepas de QC: Almacenamiento • Guardar en caldo BHI al 20% de glicerol a - 20°C. Discos y tiras de E-test: almacenamiento • Los discos y tiras de uso diario deben ser guardados a 4°C. Si no están en uso guardar a - 20°C. • Antibióticos β-lactamicos se recomienda guardar a -20°C. Control de calidad en el antibiograma: disco difusión
- 36. Principios de la difusión del antibiótico en el agar Leyes Generales de la Difusión Factores Ligados a la Difusión
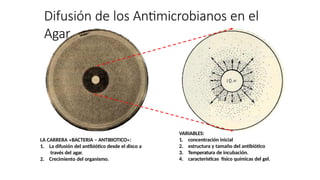
- 37. Difusión de los Antimicrobianos en el Agar VARIABLES: 1. concentración inicial 2. estructura y tamaño del antibiótico 3. Temperatura de incubación. 4. características físico químicas del gel. LA CARRERA «BACTERIA – ANTIBIOTICO»: 1. La difusión del antibiótico desde el disco a través del agar. 2. Crecimiento del organismo.
- 38. Características del borde de la zona de inhibición CIM CIM
- 39. La superficie es de 30 mm2 El volumen es de 120 mm3 La concentración en el borde del disco es: 10 g/120 mm3 = 80 g/ml Concentración del disco: 10 g Espesor del agar: 4 mm Diámetro del disco: 6 mm Agar Mueller Hinton DISCO Ampicilina 10µg 4 mm 6 mm 4 mm 80 g/ml Características del Borde de la Zona de Inhibición
- 40. 0.5 8 32 16 4 2 1 CIM µg/ml Relación entre el CIM y el diámetro de inhibición AM 3 2 1 6 8 2 25 mm 20 mm µg/ml ~ CIM
- 41. La ley de difusión de Cooper (1946) d2 = 4 D t 2,3(log C0 – log C1) d = distancia de inhibición (diámetro de la zona) D = coeficiente de difusión propio de cada antibiótico T = tiempo de difusión C0 = concentración a nivel de la fuente C1 = concentración en el borde de la zona de inhibición (concentración inhibitoria aproximada de la cepa estudiada) Cooper K.E, and Woodman D. 1946. The diffusion of antiseptic through agar gels with special reference to the agar cup assay method of estimating the activity of penicillin. J. Pathol. bacteriol. 58: 75-84. Factores relacionados a la Difusión CIM C0 C1
- 42. r2 = 9.21 Dt (logM – log 4πhDtc) Formula de Humphrey and Lightbown (1952) r = radio de la zonas de inhibición D = constante de difusión de cada antibiótico t = tiempo de inicio M = potencia del disco c = es el CIM h = profundidad del agar Humphrey, J.H., and J.W. Ligthbown. 1952. A general theory for plate assay of antibiotics with some practical applications. J. Gen. Microbiol. 7, 129-43. Factores relacionados a la Difusión CIM M C r
- 43. 10 15 20 2 1 4 8 16 32 64 128 Curva de regresión de AMPICILINA CARGA DEL DISCO: 10 ug Concentraciones criticas: 8 – 32 ug/ml Diámetros críticos: 13 – 17 mm 13 17 µg/ml y = ax + c Donde : y = diámetro (mm) x = log 2 MIC (µg/ml) Calculo del MIC 6 22 mm 25 MI C
- 44. Curva de regresión de CEFTRIAXONA 10 0 20 30 40 Determinar el MIC a partir del halo de inhibición del antibiograma por disco difusión. 0.01 0.1 1 10 Interpretación CMI (µg/ml) Diámetro (mm) Sensible ≤1 ≥ 23 Resistente ≥4 ≤ 19 PUNTOS DE CORTES DE CEFTRIAXONA: 30 mm CIM de ceftriaxona es de 0.09 µg/ml
- 45. Llamada también Cociente inhibitorio (IQ). NIVEL SERICO ó NIVEL URINARIO IT (IQ) = CONCENTRACION MINIMA INHIBITORIA Cuando mayor es el índice terapéutico, mayor es la probabilidad de que el tratamiento sea eficiente. Cuando mayor sea el nivel sérico o urinario y menor el MIC mas eficiente será la terapia. Determinación del Índice Terapéutico (IT)
- 47. Utilización del Índice Terapéutico ANTIBIOTICO Diámetro en mm Interpretación clínica MIC IT AMPICILINA 14 I 22.62 15.4 CIPROFLOXACINA 15 R 4.00 75.0 CEFTRIAXONA 20 R 2.82 283.6 GENTAMICINA 22 S 0.15 2666.6 NITROFURANTOINA 18 S 20.15 7.4 COTRIMOXAZOL 15 I 10.21 9.79 Microorganismo: Escherichia coli Muestra : Orina IT (Índice Terapéutico): Concentración A TB en orina /
- 48. CIM: Concentración mínima de antimicrobiano que inhibe el crecimiento bacteriano Capacidad del antimicrobiano para inhibir el crecimiento de las bacterias (µg/ml) 50µg/ml 25µg/ml 12.5µg/ml 0.2µg/ml 0.4µg/ml 0.8µg/ml 1.6µg/ml 3.1µg/ml 6.3µg/ml CONTROL CIM: 1.6 µg/ml Incremento de la concentración de la droga Método de macrodilución
- 49. 16 32 Relación entre el CIM y CBM CBM: Concentración mínima de antimicrobiano capaz de matar un 99.9% de la población bacteriana inicial – Refleja la posible actividad bactericida del antimicrobiano 8 4 2 1 0.5 µg/ml 8 4 2 16 32 CIM: 2 µg/ml CBM: 8 µg/ml
- 50. Cefazolina Cefuroxima Ceftazidima Cefotaxima Gentamicina Ciprofloxacina Nitrofurantoina + - 16 32 8 0.5 1 2 4 64 128 256 Ampicilina Método de microdilución
- 51. MicroScan WalkAway System (Beckman Coulter) VITEK® 2 Compact (bioMerieux-Vitek) BD Phoenix™ System (BD Diagnostic Systems) Método de automatizados con microdilución
- 55. Técnica Difusión en Gradiente (Epsilometría) Técnica que combina los principios de la difusión en disco y la dilución en agar en el estudio de la susceptibilidad in vitro Desarrollado en Suiza 1988 (E-test) Es muy simple y fácil de usar, y a diferencia de la difusión en disco, entrega un resultado cuantitativo (MIC) Mediante el uso de una innovadora técnica de química seca 60 mm 5 mm
- 56. GRADIENTE – PREFORMADO: NO SE GENERA POR DIFUSION Trasferencia inmediata desde la tira al agar en “impronta” La estabilidad de la gradiente es mantenida hasta 18 a 20 Técnica Difusión en Gradiente
- 57. d e valore s Pre calibrada con “escala continua” Técnica Difusión en Gradiente
- 58. Precisió n 2 8 Determinación del MIC 2.1 7.9 4 MIC
- 59. Interpretando la ½ Dilución Neumococo/Penicilina S: ≤ 0.064 I: 0.125 - 1 R: ≥ 2 MIC 1.5 se lee 2 µg/mL Categoría = R R I S
- 60. Tolerancia del Inoculo E. coli ATCC 25922 / Gentamicina 102 103 104 105 106 107 CFU/mL
- 61. Antibióticos con Alto Peso Molecular Disco (mm) MIC por Etest 6 4 1 6 2 0. 5 Vancomici na Disco vs Gradiente Predefinid o 1 6 1 7 1 6 1 8
- 62. Importancia en el uso de las tiras de E- test Determinación cuantitativa de la prueba de sensibilidad (MIC) para la terapia del paciente individual y dirigida. Detección exacta del mecanismo de resistencia
- 63. Cociente Breakpoint MIC (MBQ) Es calculado dividiendo el breakpoint MIC con el valor del MIC de un patógeno en particular. El antibiótico mas eficaz seria el de mas bajo MIC y el mas alto MBQ Herramienta muy practico para dirigir y afinar la terapia.
- 64. Importancia en el uso de las tiras de E-test
- 65. MIC Método de agar disco difusión Método de agar dilución Método de caldo dilución Método E-Test Principio de las Pruebas de Susceptibilidad (antibiograma)
- 66. Valores Cuantitativos HALOS DE INHIBICION (mm) o Valores de las Pruebas de Susceptibilidad (antibiograma) MIC (µg/ml) Criterios microbiológicos Criterios farmacológicas Criterios clínicos Valores Cualitativos CATEGORIAS CLINICAS: S I R
- 67. Como debemos reportar las pruebas desusceptibilidad? MIC SENSIBLE INTERMEDI O RESISTENT E
- 68. Mínima Concentración Inhibitoria (MIC) La mas baja concentración del agente antimicrobiano que inhibe el crecimiento / multiplicación bacteriano (µg/ml) Interpretación: Sensible Intermedio Resistente MIC
- 69. Importancia del MIC El conocimiento exacto y a tiempo del MIC para una variedad de antibióticos y NO solo saber que es S, I o R es importante para la decisión de elegir el antibiótico, la dosis y el esquema de dosificación que generaría un favorable resultado clínico y minimizaría la emergencia de la resistencia. George L. Drusano, M.D. Co-Director Ordway Research Institute A lbany, NY, USA